MDR 2017 / 745 Ek II Tıbbi Cihaz Teknik Dosyası, söz konusu cihazın güvenliğini ve performansını göstermek için üretici tarafından açık, iyi organize edilmiş, kolayca aranabilir ve açık bir şekilde hazırlanmış bir özet belgedir.
 MDR teknik dosya şablonu, inceleme ve onay için Onaylanmış Kuruluşa veya Yetkili Makama sunulmalıdır . Tercihen İngilizce dilinde veya bir AB Üye Devletinin resmi dilinde yapılmalıdır. Tıbbi cihazın tüm kullanım ömrü boyunca (düşük riskli cihazlar için 5 yıl ve yüksek riskli cihazlar için 16 yıl) talep üzerine mevcut olmalıdır. AB üyesi olmayan üreticiler, dosyayı AB’deki yetkili temsilcide tutmalıdır.
MDR teknik dosya şablonu, inceleme ve onay için Onaylanmış Kuruluşa veya Yetkili Makama sunulmalıdır . Tercihen İngilizce dilinde veya bir AB Üye Devletinin resmi dilinde yapılmalıdır. Tıbbi cihazın tüm kullanım ömrü boyunca (düşük riskli cihazlar için 5 yıl ve yüksek riskli cihazlar için 16 yıl) talep üzerine mevcut olmalıdır. AB üyesi olmayan üreticiler, dosyayı AB’deki yetkili temsilcide tutmalıdır.
Tıbbi cihaz sınıfı, kullanım amacı, yapısı ve veya cihazın güvenli geçmişinden bağımsız olarak, üretici, genel güvenlik ve performans gereksinimlerine uygunluğu gösteren güncel tıbbi cihaz teknik dosya belgelerine sahip olmalı ve bunları muhafaza etmelidir, MDR 2017 Ek I /745.
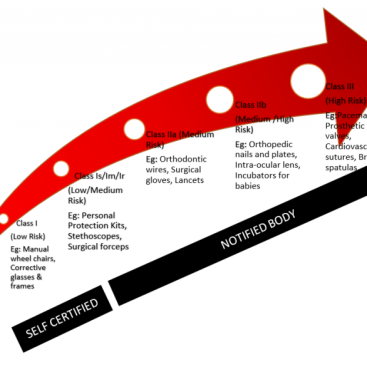
Teknik Dosya Seçim Kriterleri
Kalite Güvence ve Düzenleyici ekip üyeleri, CE İşareti için planlanan ürünler için gerekli sayıda tıbbi cihaz teknik dosyasını belirlemekte her zaman kafa karıştırır veya zorlanır.
Tıbbi cihaz teknik dosyasının veya dokümantasyonunun tamamen cihazınızla ilgili olduğunu, güvenlik ve performansın tesis edilmesi için unutmamanız tavsiye edilir. Farklı kullanım amacına, farklı sınıfa, farklı yapı malzemesine, hatta farklı tasarıma sahip ürünleri birleştiremezsiniz demektir.
Tıbbi Cihaz Teknik Dosyası Danışmanı
AB Tıbbi Cihaz CE İşareti konusunda risk analizi, validasyonlar, tasarım, raf ömrü, kullanılabilirlik, biyolojik değerlendirme, güvenlik, kimyasal özellikler ve klinik değerlendirme gibi temel teknik alanları kapsayan deneyimli bir profesyonele uzman denir. Teknik dosya hazırlamak için bu işin uzmanına yani bir danışmana ihtiyaç duyarsınız. Size bu zorlu süreçte yardımcı olabiliriz, Teknik dosya hazırlığı için doğrudan bizimle iletişime geçebilirsiniz.
- CE MDR uyarınca Gereksinim ve Tanımlama
- CE İşareti için risk sınıflandırması ve değerlendirme yolunun belirlenmesi
- Dosyaları sistematik olarak düzenlenmesi ve gözden geçirilmesi
- PMS, PMCF ve PSUR’u kapsayan Klinik Değerlendirme belgeleri
- Risk analizi
- Tıbbi Cihaz Kalite Yönetim Sistemi Uygulaması
Tıbbi Cihaz Teknik Dosya Türleri
MDR, teknik dokümantasyonunuza nelerin dahil edileceğine dair özel gereksinimler belirlemiştir.
|
SR. NO. |
TEKNİK DOSYA TÜRÜ |
UYGULANAN KURALLAR |
UYGUNLUK |
|
SINIF I |
|||
|
1. |
SINIF I İnvaziv Olmayan Cihaz |
Kural-1 Tüm İnvaziv Olmayan cihazlar sınıf I olarak sınıflandırılır | Uygunluk Değerlendirmesi Madde 52 (7). Ismarlama veya araştırma amaçlı cihazlar dışındaki sınıf I cihazların imalatçıları, Ek II ve III’te belirtilen teknik belgeleri hazırladıktan sonra, Madde 19’da atıfta bulunulan AB uygunluk beyanını düzenleyerek ürünlerinin uygunluğunu beyan eder. Onaylanmış Kuruluş katılımı zorunlu değildir.CE işareti kendi beyanı ile iliştirilebilir |
| Kural 2 – Bir sınıf IIa, sınıf IIb veya sınıf III’e bağlı olmayan, nihai infüzyon, uygulama veya vücuda giriş amacıyla kan, vücut sıvıları, hücreler veya dokular, sıvılar veya gazları kanalize etmek veya depolamak için tasarlanmış tüm invaziv olmayan cihazlar aktif cihaz; veya kan veya diğer vücut sıvılarını kanalize etmek veya depolamak veya organları, organ parçalarını veya vücut hücreleri ve dokularını depolamak için kullanılması amaçlanmayan sınıf I’dedir. | |||
| Kural 4 – Mekanik bir bariyer olarak, kompresyon veya eksüdaların emilimi için kullanılması amaçlanıyorsa, yaralı cilt veya mukoza ile temas eden tüm invaziv olmayan cihazlar. | |||
|
2. |
SINIF I İstilacı Cihaz |
Kural 5 – Cerrahi olarak invaziv cihazlar dışında, aktif bir cihaza bağlanması amaçlanmayan veya bir sınıf I aktif cihaza bağlanması amaçlanan vücut açıklıklarına ilişkin tüm invaziv cihazlar, geçici kullanım için tasarlanmışlarsa Sınıf I’dir. (Geçici’ normalde 60 dakikadan daha az sürekli kullanım için tasarlanmış anlamına gelir.) | |
| Kural 5- Ağız boşluğunda farenkse kadar, kulak zarına kadar kulak kanalında veya burun boşluğunda kullanılan ve mukoza zarı tarafından absorbe edilmeyen cihaz | |||
|
3. |
SINIF I aktif cihaz |
Kural 10 – Hastanın vücudunu görünür spektrumda aydınlatmayı amaçlayan aktif cihazlar, bu durumda sınıf I olarak sınıflandırılırlar. | |
| Kural 11- Sınıf IIa, Sınıf IIb ve Sınıf III aktif cihaz altında belirtilenler dışındaki tüm diğer yazılımlar Sınıf I olarak sınıflandırılır. | |||
| Kural 13- Diğer tüm aktif cihazlar sınıf I olarak sınıflandırılır. | |||
|
4. |
sınıf I steril ve Ölçü aleti |
Madde 52 (Madde 7) | Uygunluk Değerlendirmesi Madde 52 (7). Yeniden Kullanılabilir Cerrahi Aletler için üretici, Ek IX’un I ve III. Bölümlerinde veya Ek XI’in A Kısmında belirtilen prosedürlere göre CA’yı uygulayacaktır. Onaylanmış kuruluşun aşağıdaki durumlarda katılımı:(a) steril durumda piyasaya arz edilen cihazlar söz konusu olduğunda, steril koşulların oluşturulması, güvence altına alınması ve sürdürülmesi ile ilgili hususlar.
(b) ölçme işlevine sahip cihazlar söz konusu olduğunda, cihazların metrolojik gerekliliklere uygunluğu ile ilgili hususlar. -Steril tıbbi cihaz CE işareti için Onaylanmış kuruluş katılımı zorunludur ve cihaz Kalite Yönetim Sistemine uygun olmalıdır. – Steril durumda tedarik edilen Ölçüm cihazları için onaylanmış kuruluş sertifikası gerekir, steril olmayan cihaz için onaylanmış kuruluş katılımı gerekmez. |
|
5. |
SINIF I Cerrahi İnvaziv Cihaz |
Kural 6 – Geçici kullanıma yönelik tüm cerrahi olarak invaziv cihazlar, yeniden kullanılabilir cerrahi aletlerdir | Uygunluk Değerlendirmesi Madde 52 (7). Yeniden Kullanılabilir Cerrahi Aletler için üretici, Ek IX’un I ve III. Bölümlerinde veya Ek XI’in A Kısmında belirtilen prosedürlere göre CA’yı uygulayacaktır. Onaylanmış kuruluşun, yeniden kullanılabilir cerrahi aletler olması durumunda, cihazın yeniden kullanımı, temizlik, dezenfeksiyon, sterilizasyon, bakım ve fonksiyonel testler ve ilgili kullanım talimatları ile ilgili hususlara katılımı. |
|
Sınıf IIa |
|||
|
6. |
SINIF IIa İnvaziv Olmayan Cihaz |
Kural 2 – Kan, vücut sıvıları, hücreler veya dokular, sıvılar veya gazları nihai infüzyon, uygulama veya vücuda sokma amacıyla kanalize etmek veya depolamak için tasarlanan tüm invaziv olmayan cihazlar, aşağıdakilere bağlıysa, sınıf IIa olarak sınıflandırılır. bir sınıf IIa, Sınıf IIb veya sınıf III aktif cihaz veya bunlar, kan veya diğer vücut sıvılarını yönlendirmek veya depolamak veya organları, organ parçalarını veya vücut hücreleri ve dokularını depolamak için kullanılması amaçlanıyorsa, Sınıf IIa’ya girer. | Uygunluk Değerlendirmesi Madde 52 (6). Ismarlama veya araştırma amaçlı cihazlar dışındaki sınıf IIa cihazlarının imalatçıları, Ek IX’un I ve III. her cihaz kategorisi için en az bir temsili cihaz. VEYAİmalatçı, Ek II ve III’te belirtilen teknik belgeleri, Ek XI Bölüm 10 veya Bölüm 18’de belirtildiği gibi bir uygunluk değerlendirmesiyle birlikte hazırlamayı seçebilir. Teknik belgelerin değerlendirilmesi, her cihaz kategorisi için en az bir temsili cihaz için geçerli olacaktır.
CE işaretini iliştirmeden önce Onaylanmış kuruluş değerlendirmesi ile Uygunluk Beyanı |
| Kural 3-İnsan dokularının veya hücrelerinin, kanın, diğer vücut sıvılarının veya amaçlanan diğer sıvıların biyolojik veya kimyasal bileşimini değiştirmeye yönelik tüm invaziv olmayan cihazlar, cihazın kullanıldığı tedavi filtrasyon, santrifüj veya gaz alışverişinden oluşur, sıcaklık | |||
| Kural 4- Esas olarak yaralanmış cilt veya mukoza zarının mikro ortamını yönetmeye yönelikse, yaralı cilt veya mukoza zarını karşılayan tüm invaziv olmayan cihazlar | |||
|
7. |
SINIF IIa İstilacı Cihaz |
Kural 5- Cerrahi olarak invaziv cihazlar dışında, aktif bir cihaza bağlanması amaçlanmayan veya bir sınıf I aktif cihaza bağlanması amaçlanan vücut açıklıklarına ilişkin tüm invaziv cihazlar, kısa süreli kullanım için tasarlanmışlarsa sınıf IIa’dır. süreli kullanım (Kısa süreli’ normalde 60 dakika ile 30 gün arasında sürekli kullanım için amaçlanan anlamına gelir) | |
| Kural -5 Ağız boşluğunda farenkse kadar, kulak zarına kadar kulak kanalında veya burun boşluğunda kullanılan ve mukoza zarı tarafından emilmeye tabi olmayan cihaz, bu durumda sınıf IIa olarak sınıflandırılır | |||
| Kural 5 – Sınıf IIa, sınıf IIb veya sınıf III aktif cihaza bağlanması amaçlanan cerrahi olarak invaziv cihazlar dışındaki vücut açıklıklarına göre tüm invaziv cihazlar, sınıf IIa olarak sınıflandırılır. | |||
|
8. |
SINIF IIa Cerrahi İnvaziv Cihaz |
Kural 6- Geçici kullanım amaçlı tüm cerrahi olarak invaziv cihazlar sınıf IIa olarak sınıflandırılır | |
| Kural 7 – Kısa süreli kullanım amaçlı tüm cerrahi olarak invaziv cihazlar sınıf IIa olarak sınıflandırılır (Kısa süreli’ normalde 60 dakika ile 30 gün arasında sürekli kullanım için amaçlanan anlamına gelir) | |||
|
9. |
SINIF IIa İmplante Edilebilir Cihaz & Uzun Süreli Cerrahi İnvaziv Cihaz |
Kural 8- Dişlere yerleştirilmesi amaçlanan tüm implante edilebilir cihazlar ve uzun süreli cerrahi olarak invaziv cihazlar. | |
|
10. |
SINIF IIa Aktif Terapötik Cihaz |
Kural 9- Enerji vermek veya enerji alışverişi yapmak için tasarlanmış tüm aktif terapötik cihazlar, sınıf IIa olarak sınıflandırılır. | |
|
11. |
SINIF IIa Aktif Cihaz |
Kural 10 – Teşhis ve izleme amaçlı aktif cihazlar sınıf IIa’dır Kural 10 Aktif cihazlar, eğer insan vücudu tarafından emilecek olan enerjiyi sağlamaya yönelik iselerKural 10 Aktif cihazlar, eğer radyofarmasötiklerin in vivo dağılımını görüntüleme amaçlıysa.
Kural 10 Hayati fizyolojik süreçlerin doğrudan teşhisine veya izlenmesine izin vermeyi amaçlayan aktif cihazlar |
|
| Kural 11-Teşhis veya tedavi amaçlı kararlar almak için kullanılan bilgileri sağlamaya yönelik yazılım sınıf IIa’dır, Kural 11- Fizyolojik süreçleri izlemeye yönelik yazılımlar, sınıf IIa olarak sınıflandırılır. | |||
| Kural 12- Tıbbi ürünleri, vücut sıvılarını veya diğer maddeleri vücuda veya vücuda vermek ve/veya vücuttan çıkarmak için tasarlanan tüm aktif cihazlar, sınıf IIa olarak sınıflandırılır. | |||
|
12. |
SINIF IIa Özel durum |
Kural 16- Tıbbi cihazların dezenfeksiyonu veya sterilizasyonu için özel olarak kullanılması amaçlanan tüm cihazlar, sınıf IIa olarak sınıflandırılır. | |
| Kural 17- X-ışını radyasyonu tarafından üretilen tanısal görüntülerin kaydedilmesi için özel olarak tasarlanan cihazlar, sınıf IIa olarak sınıflandırılır. | |||
| Kural 19 – Nanomateryal içeren veya nanomalzemeden oluşan tüm cihazlar, ihmal edilebilir bir dahili maruziyet potansiyeli varsa, sınıf IIa’dır. | |||
| Kural 20 – Tıbbi ürünleri inhalasyon yoluyla vermek üzere tasarlanmış, cerrahi olarak invaziv cihazlar dışında vücut açıklıklarına göre tüm invaziv cihazlar, sınıf IIa olarak sınıflandırılır. | |||
| Kural 21- Bir vücut deliği yoluyla insan vücuduna verilmesi veya deriye uygulanması amaçlanan maddelerden veya madde kombinasyonlarından oluşan cihazlar ve İnsan vücudu tarafından emilen veya lokal olarak dağılanlar, cilde uygulandıklarında veya farenkse kadar burun veya ağız boşluğunda uygulandıklarında ve bu boşluklarda amaçlanan amaçlarına ulaştıklarında sınıf IIa olarak sınıflandırılır. | |||
|
SINIF IIb |
|||
|
13. |
SINIF IIb İnvaziv Olmayan Cihaz |
Kural 2-İnvaziv Olmayan – Kan torbaları | |
| Kural 3 İnsan dokularının veya hücrelerinin, kanın, diğer vücut sıvılarının veya vücuda implante edilmesi veya verilmesi amaçlanan diğer sıvıların biyolojik veya kimyasal bileşimini değiştirmeye yönelik tüm invaziv olmayan cihazlar, sınıf IIb olarak sınıflandırılır. | Uygunluk Değerlendirmesi Madde 52 (4). Ismarlama veya araştırma amaçlı cihazlar dışındaki sınıf IIb cihazlarının imalatçıları, Ek IX’un I ve III. genel cihaz grubu başına bir temsili cihaz VEYAÜretici, Ek XI’de belirtilen ürün uygunluk doğrulamasına dayalı bir uygunluk değerlendirmesi ile birlikte Ek X’te belirtilen tip incelemesine dayalı bir uygunluk değerlendirmesi uygulamayı seçebilir.
Madde 61:-54(1) maddesinin (b) bendinde atıfta bulunulan tüm sınıf IIb cihazlar için, imalatçı, klinik değerlendirme ve/veya araştırmadan önce, Madde 106’da atıfta bulunulan bir uzman paneline danışabilir. üreticinin amaçlanan klinik geliştirme stratejisini ve klinik araştırma önerilerini gözden geçirme amacı. İmalatçı, uzman paneli tarafından ifade edilen görüşlere gereken önemi verecektir. Onaylanmış Kuruluş tarafından CE işareti iliştirilmeden önce Uygunluk Değerlendirmeleri gereklidir. KYS uygulamasının gözden geçirilmesi, Teknik dosya, Klinik Değerlendirme, Onaylanmış kuruluş tarafından tasarımın gözden geçirilmesi. |
||
| Kural 4 Esas olarak dermis veya mukoz membranı kıran cilt yaralanmaları için kullanılması amaçlanıyorsa ve yalnızca ikincil niyetle iyileşebiliyorsa, yaralanmış cilt veya mukoza zarını karşılayan tüm invaziv olmayan cihazlar. | |||
|
14. |
SINIF IIb istilacı cihaz |
Kural 6- Cerrahi olarak invaziv cihazlar dışında, aktif bir cihaza bağlanması amaçlanmayan veya bir sınıf I aktif cihaza bağlanması amaçlanan vücut açıklıklarına ilişkin tüm invaziv cihazlar, uzun süreli kullanım için tasarlanmışsa Sınıf IIb’dir. süreli kullanım (‘Uzun süreli’ normalde 30 günden fazla sürekli kullanım için amaçlanan anlamına gelir.) | |
|
15. |
SINIF IIb Cerrahi İnvaziv cihaz |
Kural 6 İyonlaştırıcı radyasyon şeklinde enerji sağlamayı amaçlayan cerrahi olarak invaziv tüm cihazlar, bu durumda sınıf IIb olarak sınıflandırılırlar. Kural 6- Tüm cerrahi olarak invaziv cihazlar biyolojik etkiye sahiptir veya tamamen veya büyük ölçüde emilir, sınıf IIb olarak sınıflandırılırKural 6- Bir tıbbi ürünün bu şekilde uygulanması, uygulama şekli dikkate alındığında potansiyel olarak tehlikeli bir şekilde yapılıyorsa, tıbbi ürünleri bir uygulama sistemi aracılığıyla vermeyi amaçlayan tüm cerrahi olarak invaziv cihazlar sınıf IIb’dir. | |
| Kural 7 – İyonlaştırıcı radyasyon şeklinde enerji sağlamayı amaçlayan cerrahi olarak invaziv tüm cihazlar Kural 7 – İlaç vermeye yönelik tüm cerrahi invaziv cihazlar,Kural 7 – Cihazların dişlere yerleştirilmesi haricinde, vücutta kimyasal değişime uğraması amaçlanan tüm cerrahi olarak invaziv cihazlar | |||
|
16. |
SINIF IIb Aktif Terapötik Cihaz |
Kural-9 Enerjinin doğasını, yoğunluğunu ve uygulama yerini dikkate alarak, potansiyel olarak tehlikeli bir şekilde insan vücuduna enerji uygulayabilecekleri veya insan vücudunla enerji alışverişinde bulunabilecekleri tüm aktif terapötik cihazlar sınıf IIb’dir. | |
|
17. |
SINIF IIb Aktif Cihaz |
Kural 9- Aktif terapötik sınıf IIb cihazların performansını kontrol etmesi veya izlemesi amaçlanan veya bu tür cihazların performansını doğrudan etkilemesi amaçlanan tüm aktif cihazlar, sınıf IIb olarak sınıflandırılır. Kural 9- Bu tür cihazları kontrol eden veya izleyen veya performanslarını doğrudan etkileyen cihazlar da dahil olmak üzere, tedavi amaçlı iyonlaştırıcı radyasyon yayması amaçlanan tüm aktif cihazlar, sınıf IIb olarak sınıflandırılır. | |
| Kural 10 – Hayati fizyolojik parametrelerin ve bu parametrelerin varyasyonlarının doğasının izlenmesine yönelik aktif cihazlar, örneğin kardiyak performansta, solunumda, merkezi sinir sistemi aktivitesinde veya hastanın acil tehlikede olduğu klinik durumlarda teşhis amaçlıdır ve bu durumlarda sınıf IIb olarak sınıflandırılır. Kural 10 – Girişimsel radyoloji cihazları ve bu cihazları kontrol eden veya izleyen veya performanslarını doğrudan etkileyen cihazlar da dahil olmak üzere, iyonlaştırıcı radyasyon yayması amaçlanan ve teşhis veya tedavi amaçlı radyoloji amaçlı aktif cihazlar, sınıf IIb olarak sınıflandırılır. | |||
| Kural 11- Bir kişinin sağlık durumunda ciddi bir bozulmayı veya cerrahi müdahaleyi etkileyebilecek teşhis veya tedavi amaçlı kararlar almak için kullanılan bilgileri sağlamaya yönelik yazılım, sınıf IIb olarak sınıflandırılır. Kural 11- Hayati fizyolojik parametrelerin izlenmesine yönelik yazılım, bu parametrelerin varyasyonlarının doğası, hasta için ani tehlike oluşturabilecek şekilde ise, bu durumda sınıf IIb olarak sınıflandırılır. | |||
| Kural 12- Tıbbi ürünleri, vücut sıvılarını veya potansiyel olarak tehlikeli olabilecek vücuda veya vücuttan diğer maddeleri vermek ve/veya vücuttan çıkarmak için tasarlanan tüm aktif cihazlar, ilgili maddelerin, vücudun ilgili bölümünün ve uygulama şekli, bu durumda sınıf IIb olarak sınıflandırılırlar. | |||
|
18. |
SINIF IIb Özel Kurallar |
Kural 15- Doğum kontrolü veya cinsel yolla bulaşan hastalıkların bulaşmasını önlemek için kullanılan tüm cihazlar, sınıf IIb olarak sınıflandırılır. | |
| Kural 16- Kontakt lenslerin özellikle dezenfekte edilmesi, temizlenmesi, durulanması veya uygun olduğu durumlarda nemlendirilmesi için kullanılması amaçlanan tüm cihazlar, sınıf IIb olarak sınıflandırılır. Kural 16- İşlemin son noktası olarak özellikle istilacı cihazları dezenfekte etmek için kullanılması amaçlanan dezenfeksiyon solüsyonları veya yıkayıcı dezenfektörler, bu durumda sınıf IIb olarak sınıflandırılırlar. | |||
| Kural 19 – Dahili maruziyet için düşük bir potansiyele sahiplerse, nanomateryal içeren veya nanomateryalden oluşan tüm cihazlar | |||
| Kural 20 – Etki biçimlerinin uygulanan tıbbi ürünün etkinliği ve güvenliği üzerinde önemli bir etkisi olmadıkça veya tıbbi ürünleri inhalasyon yoluyla vermeyi amaçlayan cerrahi olarak invaziv cihazlar dışında, vücut açıklıklarıyla ilgili tüm invaziv cihazlar. yaşamı tehdit eden durumları tedavi etmeye yönelik, sınıf IIb olarak sınıflandırılır | |||
| Kural 21- Bir vücut deliği yoluyla insan vücuduna verilmesi veya cilde uygulanması amaçlanan ve insan vücudu tarafından emilen veya insan vücudu içinde lokal olarak dağılan maddelerden veya madde kombinasyonlarından oluşan cihazlar, sınıf IIb olarak sınıflandırılır. Sınıf III, Sınıf IIA Özel Durumda belirtilenler dışındaki tüm diğer durumlarda | |||
|
19. |
SINIF IIb İmplante Edilebilir Cihaz & Uzun Süreli Cerrahi İnvaziv Cihaz |
Kural 8- Tüm vücuda yerleştirilebilir cihazlar ve uzun süreli cerrahi olarak invaziv cihazlar, sınıf IIb olarak sınıflandırılır (‘Uzun süreli’, normalde 30 günden fazla sürekli kullanım için amaçlanan anlamına gelir.) | Uygunluk Değerlendirmesi Madde 52 (4). Sütürler, zımba telleri, diş dolguları, diş telleri, diş kronları, vidalar, kamalar, plakalar, teller, pimler, klipsler ve konektörler hariç, sınıf IIb implante edilebilir cihazlar için, Ek IX Bölüm 4’te belirtilen teknik belgelerin değerlendirmesi geçerli olacaktır. her cihaz için. |
|
SINIF III |
|||
|
20. |
SINIF III- İnvaziv Olmayan Cihaz |
Kural 3- İmplantasyon veya uygulamadan önce insan vücudundan alınan veya insan embriyoları ile in vitro olarak kullanılan insan hücreleri, dokuları veya organları ile doğrudan temas halinde in vitro olarak kullanılması amaçlanan bir madde veya maddeler karışımından oluşan tüm invaziv olmayan cihazlar vücudun içine. | Uygunluk Değerlendirmesi: – Madde 52 (3) Ismarlama veya araştırma amaçlı cihazlar dışındaki sınıf III cihazların imalatçıları, Ek IX’da belirtildiği gibi bir uygunluk değerlendirmesine tabi tutulur. Alternatif olarak, imalatçı, Ek XI’de belirtildiği gibi bir uygunluk değerlendirmesi ile birlikte Ek X’te belirtildiği gibi bir uygunluk değerlendirmesi uygulamayı seçebilir. Onaylanmış kuruluş inceleme cihazı tasarımı, CE logosunu eklemeden önce Ek II’ye göre teknik dosya.Kural 14 için: Yukarıdaki CA Madde 52 (3)’e ek olarak, Ek IX’un 5.2 Bölümünde veya Ek X’in 6. Bölümünde belirtilen Prosedür de geçerli olacaktır.
Kural 18 için:- Yukarıdaki CA Madde 52 (3)’e ek olarak, Ek IX’un 5.3 Bölümünde veya Ek X’in 6. Bölümünde belirtilen Prosedür de geçerli olacaktır. Madde 61(2)- İmalatçı, Madde 54(1)’in (b) bendinde atıfta bulunulan tüm sınıf III cihazlar için, klinik değerlendirme ve/veya araştırmadan önce, Madde 106’da atıfta bulunulan bir uzman paneline danışabilir, üreticinin amaçlanan klinik geliştirme stratejisini ve klinik araştırma önerilerini gözden geçirmek amacıyla. İmalatçı, uzman paneli tarafından ifade edilen görüşlere gereken önemi verecektir. |
|
21. |
SINIF III Cerrahi İnvaziv Cihaz |
Kural 6- Tüm cerrahi olarak invaziv cihazlar, özellikle vücudun bu bölümleriyle doğrudan temas yoluyla kalp veya merkezi dolaşım sistemindeki bir kusuru kontrol etmek, teşhis etmek, izlemek veya düzeltmek için tasarlanmıştır, bu durumda sınıf III olarak sınıflandırılırlar; Kural 6- Tüm cerrahi invaziv cihazlar, özellikle kalp veya merkezi dolaşım sistemi veya merkezi sinir sistemi ile doğrudan temas halinde kullanılmak üzere tasarlanmıştır, bu durumda sınıf III olarak sınıflandırılırlar. | |
| Kural 7 – Vücudun bu bölümleriyle doğrudan temas yoluyla özellikle kalp veya merkezi dolaşım sistemindeki bir kusuru kontrol etmek, teşhis etmek, izlemek veya düzeltmek için tasarlanmış tüm cerrahi olarak invaziv cihazlar Kural 7 – Özellikle kalp veya merkezi dolaşım sistemi veya merkezi sinir sistemi ile doğrudan temas halinde kullanılması amaçlanan tüm cerrahi olarak invaziv cihazlarKural 7 – Biyolojik etkiye sahip veya tamamen veya büyük ölçüde emilen tüm cerrahi olarak invaziv cihazlar sınıf III olarak sınıflandırılır | |||
|
22. |
Sınıf III İmplante Edilebilir Cihaz & Uzun Süreli Cerrahi İnvaziv Cihaz |
Kural 8 – Tüm implante edilebilir cihazlar ve uzun süreli cerrahi olarak invaziv cihazlar aşağıdaki durumlarda sınıf III’tür: 1) kalp, merkezi dolaşım sistemi veya merkezi sinir sistemi ile doğrudan temas halinde kullanılması amaçlanan2) biyolojik bir etkiye sahiptir veya tamamen veya büyük ölçüde emilir
3) Dişlere yerleştirilen cihazlar haricinde vücutta kimyasal değişime uğraması amaçlanır. 4) tıbbi ürünleri uygulamaya yöneliktir, 5) vücuda yerleştirilebilir aktif cihazlar veya aksesuarlarıdır. 6) meme implantları veya cerrahi ağlar, 7) vidalar, kamalar, plakalar ve aletler gibi yardımcı bileşenler hariç, tam veya kısmi eklem değiştirmeleridir. 8) spinal disk değiştirme implantları veya vidalar, kamalar, plakalar ve aletler gibi bileşenler hariç, omurgayı karşılayan implante edilebilir cihazlardır. |
|
|
23. |
Sınıf III Aktif Cihaz |
Kural 9- Vücuda yerleştirilebilir aktif cihazların performansını kontrol etmeye, izlemeye veya doğrudan etkilemeye yönelik tüm aktif cihazlar, sınıf III olarak sınıflandırılır. | |
| Kural 11-Teşhis veya tedavi amaçlı kararlar almak için kullanılan, ölüme veya kişinin sağlık durumunda geri dönüşü olmayan bir bozulmaya neden olabilecek bir etkiye sahip olan bilgileri sağlamaya yönelik yazılım, bu durumda sınıf III’e girer; | |||
|
24. |
Sınıf III Özel Kurallar |
Kural 14-. İnsan kanından veya insan plazmasından elde edilen bir tıbbi ürün de dahil olmak üzere, ayrı ayrı kullanıldığında tıbbi ürün olarak kabul edilebilecek bir maddeyi ayrılmaz bir parça olarak içeren ve cihazların yan etkisi olan tüm cihazlar, sınıf III olarak sınıflandırılır. | |
| Kural 15 – İmplante edilebilir veya uzun süreli invaziv cihazlar olan cinsel yolla bulaşan hastalıkların bulaşmasını önlemek veya kontrasepsiyon için kullanılan cihazlar sınıf III olarak sınıflandırılır. | |||
| Kural 18 – İnsan veya hayvan kaynaklı dokular veya hücreler veya bunların türevleri kullanılarak üretilen, cansız veya yaşayamaz hale getirilmiş tüm cihazlar, yalnızca sağlam deri ile temas etmesi amaçlanan cihazlar olmadıkça, sınıf III olarak sınıflandırılır. | |||
| Kural 19 – Dahili maruziyet için yüksek veya orta potansiyele sahip olmaları durumunda, nanomateryal içeren veya nanomalzemeden oluşan tüm cihazlar | |||
| Kural 21- Bir vücut deliği yoluyla insan vücuduna verilmesi veya deriye uygulanması amaçlanan ve insan vücudu tarafından emilen veya insan vücudu içinde lokal olarak dağılan maddelerden veya madde kombinasyonlarından oluşan cihazlar, eğer varsa sınıf III’tür. veya bunların metabolizma ürünleri, amaçlanan amaca ulaşmak için insan vücudu tarafından sistemik olarak emilir. Kural 21- Bir vücut deliği yoluyla insan vücuduna verilmesi veya deriye uygulanması amaçlanan ve insan vücudu tarafından emilen veya insan vücudu içinde lokal olarak dağılan maddelerden veya madde kombinasyonlarından oluşan cihazlar, eğer varsa sınıf III’tür. mide veya alt gastrointestinal sistemde amaçlanan amaçlarına ulaşırlar ve bunlar veya metabolizma ürünleri insan vücudu tarafından sistemik olarak emilir; | |||
| Kural 22- Kapalı döngü sistemleri veya otomatik harici defibrilatörler gibi, cihaz tarafından hasta yönetimini önemli ölçüde belirleyen entegre veya entegre bir teşhis işlevine sahip aktif terapötik cihazlar, sınıf III’tür. | |||
|
25. |
Sistemler ve prosedür paketleri |
Madde 22 Sistemler: – ‘sistem’, belirli bir tıbbi amaca ulaşmak için birbirine bağlanması veya birleştirilmesi amaçlanan, birlikte paketlenmiş veya paketlenmemiş bir ürün kombinasyonu anlamına gelir.Prosedür Paketleri: – ‘prosedür paketi’, belirli bir tıbbi amaç için kullanılmak amacıyla birlikte paketlenen ve piyasaya arz edilen ürünlerin bir kombinasyonu anlamına gelir; | |
| Paragraf 1. Gerçek veya tüzel kişiler, CE işareti taşıyan cihazları, aşağıda belirtilen diğer cihaz veya ürünlerle, cihazların veya diğer ürünlerin kullanım amacına uygun olarak ve kendi belirledikleri kullanım limitleri dahilinde birleştirirlerse beyanname düzenlerler. Üreticiler, bunları bir sistem veya prosedür paketi olarak piyasaya arz etmek için: (a) CE işaretini taşıyan diğer cihazlar.(b) (AB) 2017/746 Yönetmeliğine uygun olarak CE işaretini taşıyan in vitro tanı amaçlı tıbbi cihazlar.
(c) yalnızca tıbbi bir prosedürde kullanıldıkları veya sistem veya prosedür paketindeki mevcudiyetinin başka bir şekilde gerekçelendirildiği durumlarda bu ürünler için geçerli olan mevzuata uygun diğer ürünler. |
2. fıkra: 1. fıkra uyarınca yapılan açıklamada, ilgili gerçek veya tüzel kişi aşağıdakileri beyan eder: (a) Üreticilerin talimatlarına göre cihazların ve varsa diğer ürünlerin karşılıklı uyumluluğunu doğrulamışlar ve faaliyetlerini bu talimatlara göre yürütmüşlerdir.(b) sistem veya prosedür paketini paketlediler ve bir araya getirilen cihazların veya diğer ürünlerin üreticileri tarafından sağlanacak bilgileri içeren ilgili bilgileri kullanıcılara sağladılar.
(c) Cihazları ve varsa diğer ürünleri bir sistem veya prosedür paketi olarak birleştirme faaliyeti, uygun dahili izleme, doğrulama ve doğrulama yöntemlerine tabiydi. Madde, sistem veya prosedür paketi bir araya getirildikten sonra, birleştirilen cihazlara Madde 10(8) kapsamında geçerli olan süre boyunca yetkili makamların kullanımına sunulur. Bu sürelerin farklı olduğu durumlarda, en uzun süre geçerli olacaktır. Bu maddenin 1. paragrafında atıfta bulunulan sistem veya prosedür paketleri, kendi başlarına ek bir CE işareti taşımayacak, ancak bu maddenin 1. ve 3. paragraflarında atıfta bulunulan kişinin adını, tescilli ticari unvanını veya tescilli ticari markasını da taşıyacaktır. kişinin bulunduğu yerin tespit edilebilmesi için o kişiyle iletişim kurulabilecek adres olarak. |
||
| 3. Paragraf: – 1 inci fıkrada belirtilen sistemleri veya işlem paketlerini piyasaya arz amacıyla sterilize eden gerçek veya tüzel kişi, | Tercihlerine göre, Ek IX’da belirtilen prosedürlerden birini veya Ek XI Bölüm A’da belirtilen prosedürü uygulayın. Bu prosedürlerin uygulanması ve onaylanmış kuruluşun katılımı, steril ambalaj açılıncaya veya zarar görene kadar prosedürün sterilitenin sağlanmasına ilişkin yönleriyle sınırlı olacaktır. Gerçek veya tüzel kişi, sterilizasyonun üreticinin talimatlarına uygun olarak yapıldığını beyan eden bir beyan düzenler. | ||
| Para4:-Sistemin veya prosedür paketinin CE işaretini taşımayan cihazları içerdiği veya seçilen cihaz kombinasyonunun orijinal kullanım amaçları açısından uyumlu olmadığı veya sterilizasyonların üreticinin talimatlarına uygun olarak gerçekleştirilmediği durumlarda. Talimatlar. | Sistem veya prosedür paketi, bir cihaz olarak işlem görecek ve 52 nci madde uyarınca ilgili uygunluk değerlendirme prosedürüne tabi olacaktır. Gerçek veya tüzel kişi, imalatçıların üzerine düşen yükümlülükleri üstlenecektir. | ||
|
26. |
Özel Yapılmış Cihaz |
AB MDR 2017/745 EK XIII | Yetkili temsilci, Ek XIII Bölüm 1’de belirtilen bir beyan hazırlar. Uygunluk Değerlendirmesi: – Madde 52 (8) Sınıf III ısmarlama vücuda yerleştirilebilir cihazların imalatçıları, Ek IX Bölüm I’de belirtilen uygunluk değerlendirmesine tabi olacaktır. Alternatif olarak üretici, Ek XI Kısım A’da belirtildiği gibi bir uygunluk değerlendirmesi uygulamayı seçebilir. |
|
27. |
Soruşturma cihazları |
62 ila 81. Maddelerde belirtilen gereklilikleri takip edin | |