ABD FDA 510(k) Tıbbi Cihaz Danışmanlığı
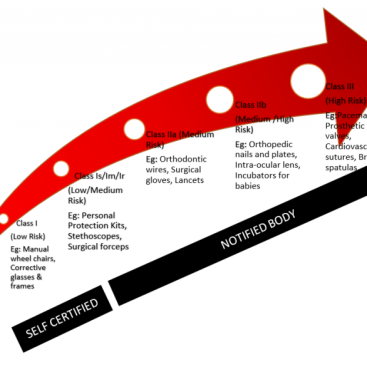
ABD FDA 510(k) Danışmanlığı hizmetimiz ile, herhangi bir tıbbi cihaz Sınıf I, Sınıf II ve Sınıf III için cihazı iyice anlayarak ve olası sorunları belirleyerek tüm süreci sorunsuz geçmenize yardımcı olur. Nitelikli ve deneyimli teknik uzmanınız, daha hızlı 510k iznini garanti eder.
Bir üretici veya spesifikasyon geliştiricisiyseniz, müşterilerin 510k Dosyasını daha hızlı hazırlayıp göndermelerini ve ilk “Refuse to Accept” (RTA) bekletmesi alma olasılıklarını düşürmek veya FDA’dan bir “Ek Bilgi” (AI) talebi nasıl desteklediğimizi anlamak için lütfen aşağıyı okuyun..
ABD FDA 510(k) Danışmanlık Faaliyetlerimiz
US FDA 510(k) Belgeleri aşağıdakileri içerir ancak bunlarla sınırlı değildir;
- Cihaz Sınıfını, ürün kodunu ve Yönetmeliğin tanımlanması
- Uygun cihaz tanımlama, doğrulama
- Uygun rehberlik ve kontrol belgelerini belirleme
- US FDA 510(k) gönderiminin uygun türünü* seçme
- Kullanım Bildirimi için Endikasyon Hazırlama
- Uygunluk beyanı
- Biyouyumluluk testlerinin tanımlanması
- Performans testinin belirlenmesi
- Örnekleme Planı
- Stabilite çalışmaları için gereklilikler
- Risk yönetimi dosyasının gözden geçirilmesi
- Sterilizasyon gereksinimleri ve uygun belgeler
- Etiketleme gereksinimleri ve etiketin gözden geçirilmesi
- ABD FDA 510(k) özeti ve doğrulaması
- Herhangi bir klinik verinin/test gereksinimlerinin tanımlanması
- Cihaza özel belge gereksinimleri – (Yazılım, EMC ve Elektrik güvenliği vb.)
- Nihai 510(k) Dosyasının İncelenmesi
- Ön başvuru (Q-submission)
- 510(k) kabul incelemesi için Refuse to Accept Politikası
- E-kopya Gönderimi
- FDA ile etkileşime geçilmesi – Gönderim sonrası aşamada İnceleme, Yorumları ve Ek Bilgi gereksinimleri yanıtlama
- Cihaz Listeleme ve Kayıt
- ABD Temsilci Hizmetleri
ABD FDA 510(k) için Danışman atamanın avantajları
- Tıbbi cihazın US FDA 510(k) gerektirdiğini ve FDA tarafından düzenlendiğini onaylayın .
- İzin almak için en doğru 510(k) yolunun belirlenmesi.
- Önemli Eşdeğerlik oluşturmak için uygun bir doğrulama aracının seçilmesi.
- FDA gereksinimlerine göre düzenleyici belgeler hazırlamak
- İyi organize edilmiş dokümantasyon
- ABD FDA 510(k) belgelerinin gözden geçirilmesi ve uyumluluk boşluklarının belirlenmesi
- Başvuru için gerekliliklerde en son trendler ve mevcut yönetmelik bilgisi
- Uygun performans testlerinin, fikir birliği standartlarının ve diğer Klinik/klinik olmayan çalışmaların gereksinimlerinin belirlenmesine yardımcı olur.
- ABD FDA510(k) danışmanı, dokümantasyondaki her adımda ve tıbbi cihaz üzerinde yapılan testlerde rehberlik edebilir ve net önerilerde bulunabilir.
- Dosyanın zamanında teslim edilmesini sağlayabilir.
- FDA ile etkileşime geçip – İnceleme, Yorumlarını Yanıtlama ve gönderi sonrası aşamada Ek Bilgi gereksinimi varsa yardımcı olabilir.
- ABD FDA 510(k) iznine kadar destek olur.