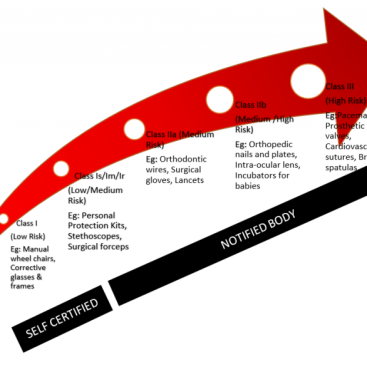
Tıbbi Cihaz üreten firmalar, tüm risk sınıfı cihazlarda deneyimli ISO 13485 Danışmanı veya bilgi birikimine sahip danışmanlık firması atamalıdır.
Tıbbi cihaz endüstrisindeki yasal gereklilikler, hasta güvenliğine artan vurgu ile sürekli olarak gözden geçirilmekte ve buna göre değiştirilmektedir.
Firmalar, çok sayıda yapılandırılmış ve yapılandırılmamış bilgi ve veriyi yönetmeli ve bunlardan değer çıkararak, sistemlerinin güncel kalmasını ve düzenleyici, bölgesel ve yerel gerekliliklerle uyumlu olmasını sağlamalıdır. Firmalar, ürünlerinin yaşam döngüsü boyunca güvenlik ve fayda-risk bilgilerini ISO 13485 gerekliliklerine uygun olarak izlemek ve izlemek için etkili sistemler uygulamalıdır.
ISO 13485 Danışmanı , uygulama sırasında MDR veya IVDR veya FDA 510k gibi ürüne özel düzenleyici gereksinimleri tanımlayabilir ve entegre edebilir . Bu, daha sonra kuruluş bir CE İşareti veya 510k Gümrük İzni almayı planladığında yardımcı olacaktır.
ISO 13485 Danışmanının Rolü ve Sorumluluğu
ISO Danışmanları , müşterilere KYS’ni planlama, geliştirme ve uygulama konusunda uzman rehberliği ile yardımcı olur:
- KYS standart gereksinimlerinin belirlenmesi
- Ürün sınıflandırmasına göre tüm yasal ve düzenleyici gereksinimlerin belirlenmesi
- Standart gereksinim aşamasını akıllıca oluşturmak için planlama
- Süreçlerin ve dokümantasyonunun geliştirilmesi ve tanımlanması
- KYS ekibine eğitim verilmesi
- KYS’nin uygulanması
- İç Kalite Denetimlerinin Yapılması
- Yönetim Gözden Geçirme Toplantıları Düzenleme
- Tüm KYS’ de sürekli iyileştirme yaklaşımı geliştirmek
- Kuruluşta uygulanan KYS’nin etkinliğini değerlendirmek
ISO 13485 Kalite El Kitabı
Kalite El Kitabı, tıbbi cihaz üreticileri için tasarlanmış bir KYS sisteminde ana belge olarak kabul edilir. AB bölgesinde kullanılmak üzere CE İşaretli tıbbi cihazlar üretiyorsanız , EN ISO 13485:2016 ile uyumluluğu kanıtlamanız gerekecektir. ISO 13485, kuruluşların Kalite El Kitabının yapısını nasıl seçtikleri veya nasıl dağıtılacağı konusunda esneklik sağlar.

ISO 13485 Zorunlu Prosedürler
ISO 13485 uygulanan kuruluş, süreçlere ve faaliyetlere dayalı olarak birçok türde prosedüre veya Standart Çalışma Prosedürlerine veya İş Talimatlarına veya Protokollere sahip olabilir.
ISO 13485:2016, standart boyunca, birden fazla yerde, kuruluşu dokümantasyonu prosedürler şeklinde tutması için doğrudan uyaran “-meli, -malı, zorunlu, dokümante edilmiş prosedürler” gibi kelimeleri kullanmıştır. Bu prosedürlere genellikle zorunlu prosedürler denir.
ISO 13485:2016 & PDCA döngüsü (Planla – Yap – Kontrol Et – Harekete Geç)
ISO 13485:2016, organizasyonun süreçlerinde sürekli mükemmellik için bir dürtünün benimsenmesine yardımcı olan PDCA döngüsünü (Planla – Yap – Kontrol Et – Harekete Geçir) takip eder. Bu yaklaşım, herhangi bir süreci daha küçük adımlara bölerek iyileştirebilir ve KYS’nin uygulanması için etkilidir ve tüm ürün gerçekleştirme sürecinin iyileştirilmesine yardımcı olur.
Ayrıca, sorunlara bir dizi çözüm sunar ve uygulama için en iyisini seçmeye yardımcı olur. Bu yöntem, çözümlerin başarılı bir şekilde uygulanması için israfı önleyerek kaynakların uygun şekilde tahsis edilmesine yardımcı olur.